
無影燈兆豐光電5月26日訊
醫(yī)療器械新規(guī)執(zhí)行相關(guān)企業(yè)需關(guān)注
M D R
前 言
醫(yī)療技術(shù)、藥品、醫(yī)療器械是構(gòu)成醫(yī)療服務(wù)體系的三大支柱。其中,醫(yī)療器械是國際公認的高新技術(shù)產(chǎn)業(yè),代表著一個國家高新技術(shù)的綜合實力。
得益于國家政策的扶持以及市場需求的增加,我國醫(yī)療器械行業(yè)銷售規(guī)模整體保持增長態(tài)勢,醫(yī)療器械出口額度逐年增加:2019年出口總額達到891.29億人民幣,同比增長達13.13%,2020年醫(yī)療儀器及機械出口總額為1259.3億人民幣,同比增長41.5%。
基于醫(yī)療器械產(chǎn)品特性,各國醫(yī)療器械的技術(shù)性貿(mào)易措施都相對比較突出,本文對即將強制執(zhí)行的歐盟《醫(yī)療器械法規(guī)(MDR)》進行研究分析并提出相關(guān)技術(shù)性貿(mào)易措施應(yīng)對建議,供出口企業(yè)參考。

(EU 2017/745)
MDR
據(jù)悉, 歐盟將于2021年5月26日強制執(zhí)行新版醫(yī)療器械法規(guī)MDR(EU 2017/745)。
2017年5月5日,歐盟正式發(fā)布新版醫(yī)療器械法規(guī)MDR(EU 2017/745),取代舊的醫(yī)療器械指令MDD( 93/42/EEC)。新舊法規(guī)交替過渡期為三年。
2019年,海關(guān)總署組織技術(shù)性貿(mào)易措施研究評議基地成功應(yīng)對歐盟MDR新規(guī),促使歐盟在2020年4月24日正式宣布將 《醫(yī)療器械法規(guī)(MDR)》強制實施日期推遲一年,這為中國醫(yī)療器械生產(chǎn)企業(yè)爭取到了寶貴的緩沖時間,但強制執(zhí)行日期2021年5月26日 已近在眼前。
一、新法規(guī)下歐盟醫(yī)療器械的主要分類
根據(jù)歐盟新頒布的醫(yī)療器械法規(guī)《醫(yī)療器械法規(guī)》(2017/745,MDR)和《體外診斷器械法規(guī)》(2017/746,IVDR),歐盟將醫(yī)療器械分為兩大類別:醫(yī)療器械MD和體外診斷器械IVD。MDR法規(guī)執(zhí)行時間為2021年5月26日,IVDR法規(guī)執(zhí)行時間為2022年5月26日。
侵入式醫(yī)療器械MD根據(jù)風(fēng)險等級再細分為 I、IIa、 IIb、III類;非侵入式體外診斷器械IVD依據(jù)風(fēng)險等級由低到高細分為A、B、C、D四類。
二、新歐盟 醫(yī)療器械法規(guī)MDR的主要變化
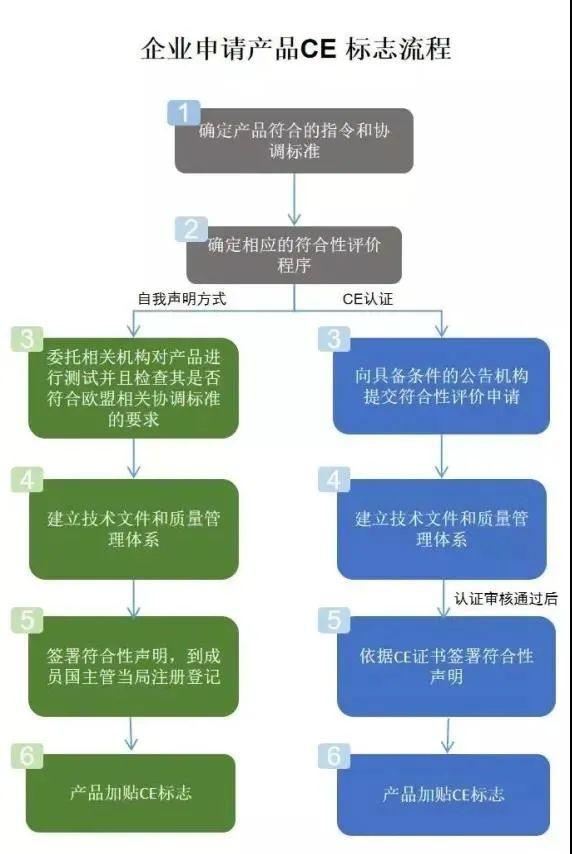
總體來說,歐盟MDR新規(guī)更加關(guān)注臨床性能、更好的醫(yī)療器械可追溯性和對患者更大的透明度,具體變化有:醫(yī)療器械的范圍擴大;提出醫(yī)療器械新概念和定義;設(shè)立中央電子資料庫(Eudamed);設(shè)立產(chǎn)品獨立的產(chǎn)品識別碼(UDI);完善了醫(yī)療器械的通用安全和性能要求;加強對技術(shù)文件的要求;加強器械上市后的監(jiān)管;完善臨床評價相關(guān)要求;對授權(quán)認證機構(gòu)(NB)提出嚴格要求等,這意味著對進入歐洲市場的醫(yī)療器械將實施更嚴格的限制,對行業(yè)企業(yè)提出了更高的要求。
三、相關(guān)企業(yè)應(yīng)該做好應(yīng)對準備
歐盟MDR新規(guī)將給中國出口企業(yè)帶來成本增加、認證周期拉長和合規(guī)風(fēng)險增加等問題,建議相關(guān)企業(yè)做好相應(yīng)準備。一是加大MDR新規(guī)關(guān)注力度并做好CE認證更新。過渡期前簽發(fā)的CE證書有效期不超過5年,并于2024年5月27日失效,而2021年5月26日后申請CE認證的,必須按照MDR法規(guī)要求辦理,并由授權(quán)NB簽發(fā);二是樹立質(zhì)量意識和責(zé)任意識,按照MDR法規(guī)要求合規(guī)生產(chǎn),保障產(chǎn)品和標準的符合性;三是與國外客戶加強聯(lián)絡(luò)溝通,明確生產(chǎn)標準和認證要求以避免后續(xù)認證和價格糾紛。
免責(zé)聲明:本站部份內(nèi)容系轉(zhuǎn)載,不代表本網(wǎng)站贊同其觀點;如涉及內(nèi)容、版權(quán)等問題,請在30日內(nèi)聯(lián)系,我們將在第一時間刪除內(nèi)容!